TB-500
Klinischer Überblick
Überblick
TB-500 ist der Handelsname, unter dem ein synthetisches Peptid vertrieben wird, das eng mit dem endogenen humanen Peptid Thymosin beta‑4 (Tβ4) verwandt ist. Thymosin beta‑4 ist ein natürlich vorkommendes, 43‑aminosäurehaltiges Protein, das in vielen Geweben exprimiert wird und eine Rolle bei Zellmigration, Gewebereparatur, Angiogenese und Entzündungsmodulation spielt. TB‑500 wird als synthetische, kürzere, biologisch aktive Sequenz oder als synthetisches Analogon von Teilen der Tβ4‑Sequenz beschrieben. Es wird in Forschungs- und Veterinärkreisen sowie in der „Leistungssteigerungs‑Community“ verwendet, ursprünglich wegen berichteter pro‑regenerativer Effekte (Wundheilung, Reduktion von Entzündung, Förderung der Gewebe‑Reparatur).
Wegen unzureichender, groß angelegter klinischer Studien und fehlender Zulassung durch große Behörden (z. B. EMA, FDA) ist TB‑500 nicht als zugelassenes Arzneimittel für Menschen etabliert. Es existieren primär präklinische Daten (in vitro und Tiermodelle) sowie eine Vielzahl an anekdotischen Berichten über den Einsatz beim Menschen und bei Tieren.
Chemische Eigenschaften
- Chemische Formel: Nicht zutreffend in der Form einer kleinen organischen Verbindung; TB‑500 ist ein Peptid und hat daher eine Sequenz aus Aminosäuren. Kommerzielle Angaben zur exakten Sequenz variieren; typischerweise wird TB‑500 als Fragment oder Analogon von Thymosin beta‑4 beschrieben.
- Molekulargewicht: Variiert je nach exakter Sequenz und Modifikationen; Peptid‑Typen im Bereich der Tβ4‑Fragmente liegen typischerweise im Bereich von einigen Hundert bis einigen Tausend Dalton.
- Struktur:
- Endogenes Thymosin beta‑4: ein linearer Polypeptidkette von 43 Aminosäuren (N‑terminal acetyliert).
- TB‑500: meist als kürzeres synthetisches Peptid mit einer konservierten, biologisch aktiven Region von Tβ4 beschrieben; genaue Sequenz und post‑translationalen Modifikationen sind produktabhängig.
- Löslichkeit: Peptide wie TB‑500 sind in wässrigen Lösungen löslich; für parenterale Applikation werden sie meist als gefriergetrocknetes Pulver (Lyophilisat) geliefert und vor Injektion in steriles Wasser oder geeignete Lösungsmittel reconstituiert.
- Stabilität: Peptide sind empfindlich gegenüber Proteasen; Stabilität hängt von Lagerung (kühl, lichtgeschützt), pH und Lösungsmittel ab. Lyophilisierte Formulierungen sind stabiler als in Lösung.
Tabelle: Allgemeine physikochemische Merkmale (typisch, produktabhängig)
| Eigenschaft | Beschreibung |
|---|---|
| Typ | Synthetisches Peptid (Analog/Fragment von Thymosin beta‑4) |
| Molekulargewicht | Produktabhängig (häufig mehrere hundert bis tausend Da) |
| Löslichkeit | Wasserlöslich (in wässrigen Puffern) |
| Lagerung | Kühl und trocken; lyophilisiert stabiler |
| Herstellungsverfahren | Festphasen‑Peptidsynthese (SPPS) üblich |
Hinweis: Wegen variabler Quellen und fehlender standardisierter Produktinformationen existieren keine einheitlichen, offiziellen pharmakognostischen Daten vergleichbar mit zugelassenen Arzneistoffen.
Wirkmechanismus
Der Wirkmechanismus von TB‑500 wird aus den bekannten biologischen Aktivitäten von Thymosin beta‑4 abgeleitet. Thymosin beta‑4 ist ein multifunktionales Aktofilament‑assoziiertes Peptid mit zahlreichen zellulären Effekten. Wichtige postulierte Mechanismen:
- Bindung an G‑Actin und Förderung der Aktin‑Dynamik:
- Tβ4 bindet monomeres Aktin (G‑Actin) und reguliert die Verfügbarkeit von Aktin für Polymerisation. Dies moduliert Zellform, Zellmigration und Zytoskelett‑Remodelling – Prozesse, die für Wundheilung und Zellwanderung zentral sind.
- Förderung von Zellmigration und Angiogenese:
- Tβ4 erhöht motilitätsbezogene Signalwege in Endothelzellen und Fibroblasten, unterstützt die Bildung neuer Blutgefäße (Angiogenese) und erleichtert die Rekrutierung von Reparaturzellen an Verletzungsstellen.
- Anti‑apoptotische und zellschützende Effekte:
- In verschiedenen Modellen wurden antiapoptotische Effekte beobachtet, z. B. durch Reduktion von oxidativem Stress oder Modulation pro‑/antiapoptotischer Proteine.
- Entzündungsmodulation:
- Tβ4 scheint Entzündungsantworten zu modulieren, indem es die Expression von Zytokinen beeinflusst und die Infiltration proinflammatorischer Zellen reduzieren kann.
- Förderung von Differenzierung und Re‑Epithelialisierung:
- Bei Haut‑ und Hornhautverletzungen wurde eine beschleunigte Epithelneubildung beschrieben.
TB‑500 wird angenommen, diese Effekte ähnlich wie Tβ4 zu vermitteln, möglicherweise mit verbesserter pharmakokinetischer Stabilität oder bioverfügbarkeit. Die genauen Signalwege sind teilweise noch Gegenstand der Forschung; Effekte auf integrinvermittelte Signale, MAP‑Kaskaden, VEGF‑assoziierte Pfade und andere pro‑regenerative Transkriptionsprogramme wurden diskutiert.
Wichtig: Viele Daten stammen aus in vitro‑Experimenten und Tierstudien; eine direkte Übertragbarkeit dieser Mechanismen auf den klinischen Menschengebrauch ist nicht vollständig belegt.
Medizinische Informationen
Anwendungsgebiete (experimentell/erforscht):
- Wundheilung und Gewebereparatur:
- Tiermodelle zeigen beschleunigte Heilung von Hautwunden, Sehnenverletzungen, Muskelschäden und Hornhautverletzungen.
- Kardiovaskuläre Reparatur:
- Präklinische Daten deuten darauf hin, dass Tβ4 die Rekrutierung von Vorläuferzellen und die Remodellierung nach Myokardinfarkt positiv beeinflussen kann.
- Ophthalmologie:
- Studien und Fallberichte untersuchen die Verwendung bei Hornhautdefekten und Ulzera.
- Orthopädie und Sportverletzungen:
- Tier‑ und wenige Human‑Fallberichte beschreiben verbesserte Sehnenheilung, reduzierte Fibrose und schnellere Funktionserholung.
- Neuroprotektion und Regeneration:
- Einige Modelle legen nahe, dass Tβ4 neuroprotektive Effekte haben und neuronale Reparatur fördern könnte.
Klinische Studien:
- Der Großteil der Evidenz für TB‑500 beruht auf präklinischen Studien. Für Thymosin beta‑4 selbst existieren einige frühe Phase‑I/II Studien in speziellen Indikationen, jedoch sind die Daten begrenzt und heterogen.
- Für TB‑500 als kommerzielles Produkt sind kontrollierte, groß angelegte klinische Studien zur Wirksamkeit und Sicherheit beim Menschen weitgehend nicht verfügbar.
Dosis und Verabreichung:
- In der Praxis (Nicht‑zugelassene Anwendungen) wird TB‑500 üblicherweise parenteral (intramuskulär oder subkutan) injiziert. Dosierungsregime variieren stark in der Literatur bzw. bei Anwenderberichten.
- Standardisierte, evidenzbasierte Dosierungen für humane Indikationen existieren nicht; Anwendungen sind experimentell und oft empirisch.
Kontraindikationen:
- Schwangerschaft und Stillzeit: Daten fehlen; mögliche Risiken unbekannt — vorsorglich kontraindiziert.
- Personen mit aktiven malignen Erkrankungen: Aufgrund pro‑angiogener Effekte sollten Patienten mit bekannter oder vermuteter Tumorerkrankung TB‑500 meiden, bis Sicherheit geklärt ist.
- Allergie/Überempfindlichkeit gegen Peptidbestandteile: potentielles Risiko für Immunreaktionen.
Sicherheitsprofil
Datenlage:
- Die Sicherheitsdaten für TB‑500 beim Menschen sind limitiert. Vornehmlich stehen präklinische Toxicity‑Profile und anekdotische Berichte zur Verfügung; systematische, kontrollierte Humanstudien sind rar.
Gemeldete Nebenwirkungen (aus Fallberichten, anekdotischen Quellen und Tierstudien):
- Lokalreaktionen an der Injektionsstelle (Schmerzen, Rötung, Schwellung).
- Müdigkeit oder allgemeines Unwohlsein in einzelnen Berichten.
- Potentielle Veränderungen im Blutbild oder biochemischen Parametern bei Langzeitanwendung sind nicht systematisch dokumentiert.
- Immunogene Reaktionen: Wie bei fremden Peptiden besteht die Möglichkeit der Antikörperbildung und allergischer Reaktionen.
- Theoretische Risiken:
- Förderung von Angiogenese und Zellproliferation könnte theoretisch die Progression bereits bestehender Tumoren unterstützen. Dieser potenzielle onkologische Risikofaktor ist nicht abschließend untersucht.
- Systemische Effekte auf Gefäß‑ oder Blutgerinnungssysteme sind nicht gut charakterisiert.
Pharmakokinetik:
- Nur begrenzte Daten; Peptide werden häufig schnell im Plasma metabolisiert (Proteasen) und haben kurze Halbwertszeiten, sofern sie nicht durch Modifikationen stabilisiert sind.
- Verteilung, Metabolisierung und Eliminationswege von TB‑500 sind nicht ausreichend dokumentiert.
Wechselwirkungen:
- Keine standardisierten Daten zu Medikamentenwechselwirkungen. Vorsicht bei gleichzeitiger Anwendung mit anderen Substanzen, die Wundheilung, Angiogenese oder Immunantworten beeinflussen.
Risikomanagement:
- Aufgrund der unsicheren Sicherheitslage ist bei experimentellem Einsatz engmaschige ärztliche Überwachung, Laborkontrollen und ein individuelles Nutzen‑Risiko‑Assessment notwendig.
- Besondere Vorsicht bei Patienten mit Krebsanamnese, Autoimmunerkrankungen oder schwerer Leber‑/Niereninsuffizienz.
Rechtsstatus
- Zulassung: TB‑500 ist in den meisten Ländern nicht als Medikament für den menschlichen Gebrauch zugelassen. Es existieren keine umfassenden behördlich genehmigten Indikationen.
- Verkauf: Viele Anbieter verkaufen TB‑500 als „Research Chemical“, „Veterinary Use“ oder „Not for Human Consumption“. Solche Kennzeichnungen spiegeln den rechtlichen Status wider und dienen dazu, regulatorische Vorschriften zu umgehen.
- Sportrechtliche Bestimmungen:
- Die Welt‑Anti‑Doping‑Agentur (WADA) führt Thymosin beta‑4 und verwandte Peptide in ihrer Verbotsliste (als Peptidhormone oder Wirkstoffklassen aufgeführt). Athleten, die unter Anti‑Doping‑Regeln stehen, dürfen diese Substanzen nicht verwenden.
- Verschreibung/Apothekenstatus:
- Da keine breite Zulassung existiert, ist TB‑500 in der Regel nicht verschreibungsfähig als standardisiertes Arzneimittel. In einigen Ländern können Zugangswege über klinische Studien oder Sondergenehmigungen möglich sein.
- Gesetzliche Kontrolle:
- TB‑500 ist in den meisten Rechtsordnungen nicht als kontrollierte Droge gelistet, jedoch können Import‑ und Vertriebsregelungen (z. B. Arzneimittelgesetze, Tierarzneimittelgesetze) Anwendung finden. Der Verkauf als „Forschungschemikalie“ entbindet Anbieter nicht von allen regulatorischen Anforderungen.
Schlussbemerkungen
TB‑500 ist ein synthetisches Peptid, das aufgrund seiner engen Verbindung zu Thymosin beta‑4 und der daraus abgeleiteten biologischen Effekte an Interesse für Regenerations‑ und Reparaturprozesse gewonnen hat. Die vorliegenden Daten stammen überwiegend aus in vitro‑Experimenten und Tiermodellen; hochwertige randomisierte, kontrollierte Studien beim Menschen fehlen größtenteils. Daraus folgt, dass Aussagen über Wirksamkeit und Langzeitsicherheit beim Menschen spekulativ sind.
Vor dem Einsatz von TB‑500 — insbesondere außerhalb kontrollierter Forschungsumgebungen — sollten medizinische Fachpersonen eine evidenzbasierte Nutzen‑Risiko‑Abwägung treffen. Personen mit Wettbewerbsstatus im Sport sollten beachten, dass Thymosin beta‑4 und verwandte Peptide auf Dopinglisten stehen. Aufgrund unsicherer Qualitätskontrolle bei nicht regulierten Produkten bestehen zusätzliche Risiken durch Verunreinigungen, falsche Dosierungen und falsche Produktdeklarationen.
Literaturhinweis (selektiv): Für detaillierte Mechanismen und präklinische Daten sind peer‑reviewte Studien zu Thymosin beta‑4 sowie Übersichtsartikel über peptidbasierte Regenerationsstrategien empfehlenswert. Klinische Anwendungsempfehlungen und regulatorische Informationen sollten den aktuellen Veröffentlichungen von Gesundheitsbehörden und Fachgesellschaften entnommen werden.
science Chemische Eigenschaften
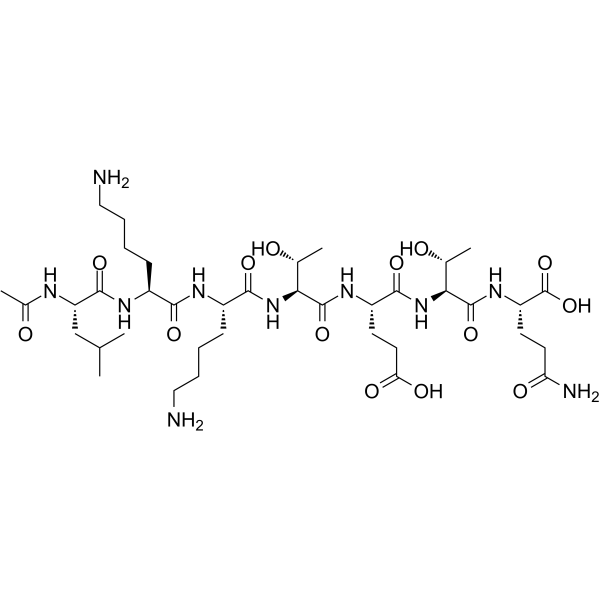
2D-Struktur
Molekularformel
scienceC208H344N60O63S2
Molare Masse
science4963.5 g/mol
Halbwertszeit
science7-10 Tage
Anabol/Androgen Verhältnis
scienceN/A (Peptid)
bolt Wirkmechanismus
TB-500 ist eine synthetische Version von Thymosin Beta-4. Es fördert Zellmigration und hilft bei Muskelflexibilität und Verletzungsheilung.
- Zellmigration: Hilft Zellen, zu Verletzungsstellen zu wandern.
- Flexibilität: Reduziert Entzündungen und verbessert Flexibilität.
Reinheit
Auf Reinheit der Quelle achten.
medication Dosierungsprotokoll
| Erfahrungsstufe | Tagesdosis | Zyklusdauer |
|---|---|---|
| Laden | 5-10 mg | 4 Wochen |
| Erhaltung | 2-5 mg | Laufend |
* Wirkt gut in Synergie mit BPC-157.
security Sicherheitsprofil
warning Häufige Nebenwirkungen
-
bedtime
Müdigkeit
Vorübergehende Müdigkeit nach Injektion.
dangerous Schwere/Seltene Nebenwirkungen
shopping_cart Verwandte Produkte
Haftungsausschluss: Dieser Inhalt dient nur zu Informations- und Bildungszwecken. Er stellt keine medizinische Beratung dar.